
发布时间:2024-06-28 08:49:40 浏览次数:907次
最近,细菌的抗生素耐药性增强以及新型抗生素的匮乏促使农业、医药和一些食品行业重新流行起噬菌体抗菌的方法(图1)。利用噬菌体对细菌进行敏感和特异性检测也引人关注。人们正在开发多种检测方法,包括基于噬菌体诱导的裂解、噬菌体扩增、报告基因传递、细胞表面结合蛋白和生物传感器的系统1。使用天然或改良烈性噬菌体的噬菌体疗法显示出令人鼓舞的治疗效果,并且正在进行受控的临床试验2,3。例如,用于治疗铜绿假单胞菌耳部感染的噬菌体混合物显示出明显的功效和安全性4。目前,一项涉及三个欧洲国家的I/II期临床试验,正在研究噬菌体用于治疗感染大肠杆菌和铜绿假单胞菌的烧伤创面的安全性和有效性(称为PhagoBurn临床试验)。在食品安全和农业方面,噬菌体技术的应用速度越来越快,有几种批准的产品可以商业化。例如用于保护加工食品免受李斯特菌侵害的LISTEX P100和ListShield。
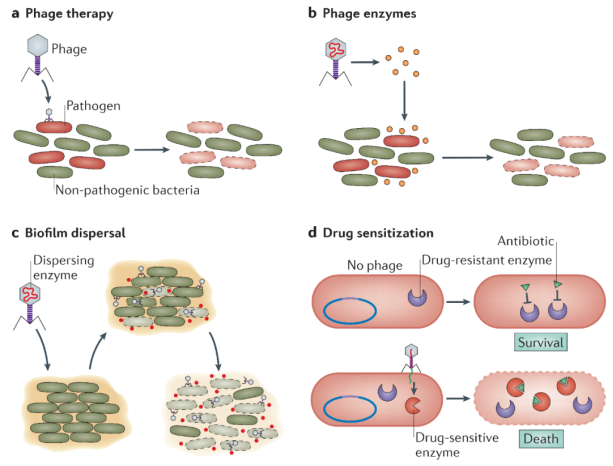
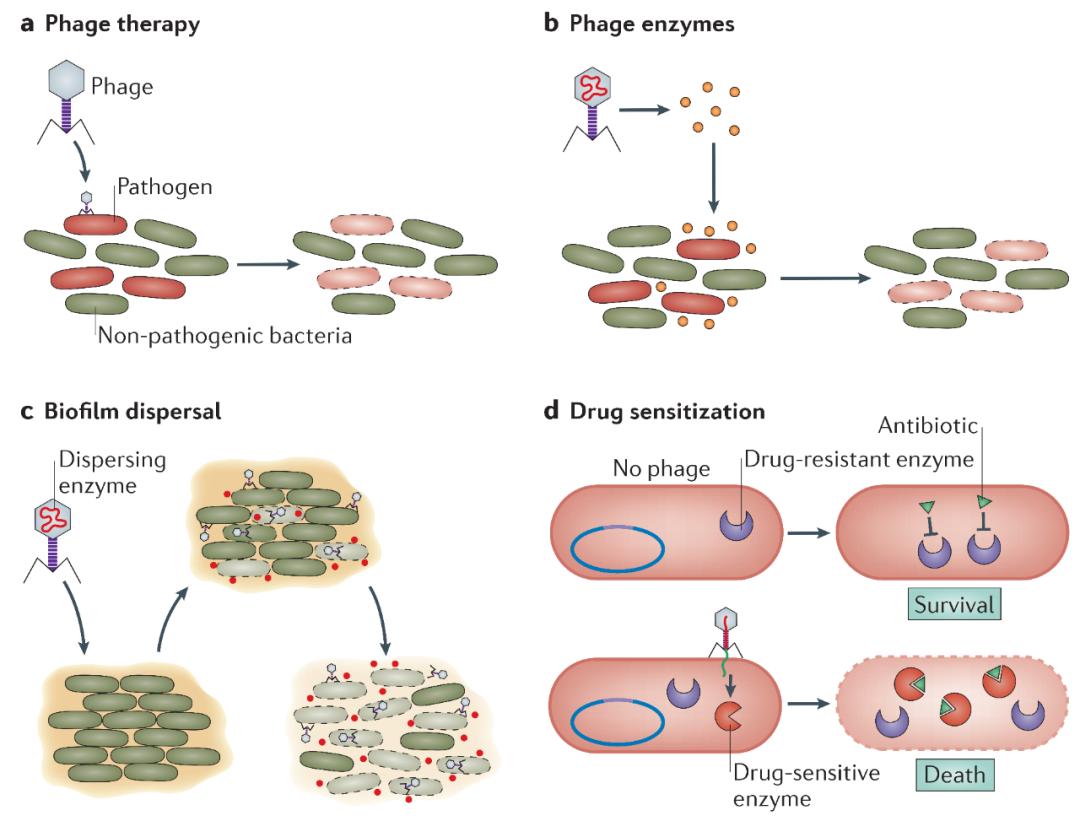
图1:—些基于噬菌体的抗菌方法
噬菌体及其产物提供了—种新的抗菌策略。
a噬菌体的特异性可用于噬菌体治疗,通过噬菌体靶向攻击特定的细菌病原体;b噬菌体的产物(例如酶)可用于针对特定的细菌,包括病原体;c噬菌体可以通过靶向嵌入细菌中的某些结构来破坏生物膜,并且可以被设计用来释放降解生物被膜基质的特定酶;d噬菌体可用于敏化抗生素抗性细菌。例如,噬菌体可以将抗生素敏感基因导入耐药宿主,这种策略可以与抗生素治疗相结合。
越来越多的使用噬菌体产品或工程噬菌体的新抗菌方法正在开发中(图1)。大量研究集中在裂解酶上,裂解酶是在噬菌体复制过程中参与细胞裂解的肽聚糖水解酶。在革兰氏阴性细菌中,外膜还必须通过复合物(称为spanins)破坏,并融合两个膜。裂解酶通常由酶活性结构域和细胞壁结合结构域组成。裂解酶种类多样,大多数裂解酶具有物种特异性,有些则可感染多个物种。裂解酶的模块化促进了不同域的“混合和匹配”,以增加活性并改变宿主范围5。通过将裂解酶融合到其他结构域,可以将裂解酶穿过革兰氏阴性外膜或传递到真核细胞中以靶向细胞内细菌。目前正在进行局部和静脉内使用裂解酶控制人类金黄色葡萄球菌感染的l期和ll期临床试验,并且已经在各种感染模型中进行了临床前试验。第一种上市的裂解酶Staphefekt可用于治疗由金黄色葡萄球菌引起的人类皮肤感染。
使用裂解酶的一种补充方法涉及利用尾钉或可扩散的多糖解聚酶,这可以降低如胞外多糖(EPSs)和脂多糖(LPSs)等表面聚合物的水平。去除多糖可以破坏生物膜,降低毒力并通过宿主免疫系统协助清除细菌。在此前提下,T7噬菌体被设计为在大肠杆菌生物膜感染期间表达EPS降解酶。细胞裂解释放出EPS降解酶,有助于噬菌体感染并增强抗生物膜和抗菌作用(图1)。噬菌体对其靶细菌的特异性通常被认为具有治疗优势,因为这可以限制对有益微生物的附带损害。对于可降解EPS的T7噬菌体,可通过从T3噬菌体引入基因1.2来扩大其宿主范围,从而增强其实用性,能够感染含有F质粒的大肠杆菌。还可以利用进化来选择改变的受体识别和宿主范围。例如,λ噬菌体的体外进化可以识别新的孔蛋白受体—外膜蛋白F(OmpF)。在自然环境中,博德特氏菌噬菌体BPP-1通过产生多样性、位点特异性、易错的逆转录来加速其尾部纤维进化,从而改变其宿主范围6。噬菌体的特异性及其DNA传递效率已被用于注射致命基因的细菌,这些基因编码内切酶、胆碱、毒素-抗毒素系统的毒素或浓缩DNA的蛋白质(例如SASPject;Phico Therapeutics,Cambridge,UK)。
噬菌体还可以提高抗生素功效(图1)。例如,抗生素可以偶联到噬菌体上,使其能够传递到特定的细菌细胞,并导致局部药物浓度的增加。此外,可以通过使用噬菌体注射突变基因的敏感等位基因(例如rpsL和gyrA)来克服抗生素耐药性,以恢复药效7。另外,调控基因的传递可以以一种特定的方式重新编程细胞。例如,引入抑制应激反应的基因(如LexA)、改善药物摄取的基因(如OmpF)或抑制生物膜产生的基因(如CSRA)可以提高大肠杆菌对抗生素的敏感性8。因此,噬菌体提供了广泛的潜在方法来解决细菌感染和抗生素耐药性。但是,噬菌体工程依然面临一些需要解决的法律问题。
参考文献
1. Schmelcher, M. & Loessner, M. J. Application of bacteriophages for detection of foodborne pathogens. Bacteriophage 4, e28137 (2014).
2. Chan, B. K., Abedon, S. T . & Loc-Carrillo, C. Phage cocktails and the future of phage therapy. Future Microbiol. 8, 769–783 (2013).
3. Nobrega, F . L., Costa, A. R., Kluskens, L. D. & Azeredo, J. Revisiting phage therapy: new applications for old resources. T rends Microbiol. 23, 185–191 (2015).
4. Wright, A., Hawkins, C. H., Anggard, E. E. & Harper, D. R. A controlled clinical trial of a therapeutic bacteriophage preparation in chronic otitis due to antibiotic-resistant Pseudomonas aeruginosa; a preliminary report of efficacy. Clin. Otolaryngol. 34, 349–357 (2009).
5. Roach, D. R. & Donovan, D. M. Antimicrobial bacteriophage-derived proteins and therapeutic applications. Bacteriophage 5, e1062590 (2015).
6. Liu, M. et al. Reverse transcriptase-mediated tropism switching in Bordetella bacteriophage. Science 295, 2091–2094 (2002).
7. Edgar, R., Friedman, N., Molshanski-Mor, S. & Qimron, U. Reversing bacterial resistance to antibiotics by phage-mediated delivery of dominant sensitive genes. Appl. Environ. Microbiol. 78, 744–751 (2012).
8. Lu, T . K. & Collins, J. J. Engineered bacteriophage targeting gene networks as adjuvants for antibiotic therapy. Proc. Natl Acad. Sci. USA 106, 4629–4634 (2009).

服务热线(期待您的来电):

地址:湖北省武汉市江夏区郑店街道光谷南大健康产业园30号

邮箱:HBZW_Chenzaiwei@163.com
扫一扫关注我们
